Méthodes de production d'hydrogène en conditions industrielles
Extraction par conversion de méthane
... De l'eau à l'état de vapeur, préchauffée à 1000 degrés Celsius, est mélangée avec du méthane sous pression et en présence d'un catalyseur. Cette méthode est intéressante et éprouvée, il faut également noter qu'elle est constamment améliorée: la recherche de nouveaux catalyseurs, moins chers et plus efficaces, est en cours.
Considérez la méthode la plus ancienne de production d'hydrogène - gazéification du charbon
... À condition qu'il n'y ait pas d'accès à l'air et à une température de 1300 degrés Celsius, le charbon et la vapeur d'eau sont chauffés. Ainsi, l'hydrogène est déplacé de l'eau et le dioxyde de carbone est obtenu (l'hydrogène sera en haut, le dioxyde de carbone, également obtenu à la suite de la réaction, est en bas). Ce sera la séparation du mélange gazeux, tout est très simple.
Obtention d'hydrogène par électrolyse de l'eau
est considérée comme l'option la plus simple. Pour sa mise en œuvre, il est nécessaire de verser une solution de soude dans le récipient, et également d'y placer deux éléments électriques. L'un sera chargé positivement (anode) et l'autre négativement (cathode). Lorsqu'un courant est appliqué, l'hydrogène ira à la cathode et l'oxygène à l'anode.
Obtention d'hydrogène par la méthode oxydation partielle
... Pour cela, un alliage d'aluminium et de gallium est utilisé. Il est placé dans l'eau, ce qui conduit à la formation d'hydrogène et d'alumine au cours de la réaction. Le gallium est nécessaire pour que la réaction se déroule pleinement (cet élément empêchera l'aluminium de s'oxyder prématurément).
Pertinence récemment acquise méthode d'utilisation de la biotechnologie
: en cas de manque d'oxygène et de soufre, les chlamydomonas commencent à libérer de l'hydrogène de manière intensive. Un effet très intéressant qui est actuellement activement étudié.

N'oubliez pas une autre méthode ancienne et éprouvée de production d'hydrogène, qui consiste à utiliser différents éléments alcalins
et de l'eau. En principe, cette technique est réalisable en laboratoire à condition que les mesures de sécurité nécessaires soient en place. Ainsi, au cours de la réaction (elle se déroule avec chauffage et avec des catalyseurs), il se forme un oxyde métallique et de l'hydrogène. Il ne reste plus qu'à le collecter.
Obtenez de l'hydrogène en interaction de l'eau et du monoxyde de carbone
possible uniquement dans un environnement industriel. Du dioxyde de carbone et de l'hydrogène se forment, le principe de leur séparation est décrit ci-dessus.

Comment obtenir de l'hydrogène en toute sécurité à la maison?
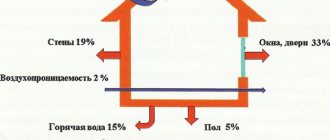
Ces questions sont touchantes, car il semble à un homme ordinaire dans la rue qu'il est assez simple d'obtenir de l'hydrogène, et pourtant cela, bien que cela puisse être fait dans des conditions normales, est encore assez dangereux. La première chose que vous devez savoir est que vous devez faire de telles expériences uniquement à l'air libre (à l'extérieur), car l'hydrogène est un gaz très, très léger (environ 15 fois plus léger que l'air standard) et il s'accumule près du plafond, formant un mélange hautement explosif. Si toutes les mesures nécessaires sont prises pour éviter les moments problématiques, il est alors possible d'effectuer la réaction de l'interaction de l'alcali et de l'aluminium.
Nous prenons un flacon (le meilleur de tous) ou une bouteille en verre de 1/2 litre, un bouchon (au milieu du trou), un tube pour éliminer l'hydrogène, 10 grammes d'aluminium et de vitriol (cuivre), du sel de table (environ 20 grammes), de l'eau en une quantité de 200 ml. et une bille (caoutchouc) pour collecter l'hydrogène. Nous achetons du vitriol dans les magasins de jardinage, et les canettes de bière ou le fil de fer peuvent très bien servir de matières premières en aluminium. Bien sûr, l'émail est d'abord éliminé par cuisson, il faut de l'aluminium pur, sans impuretés.
Pour 10 grammes de vitriol, 100 ml d'eau sont respectivement prélevés et une deuxième solution est préparée - pour 20 grammes de sel, 100 ml d'eau iront. La nuance des solutions sera la suivante: vitriol - bleu, sel - incolore. Ensuite, nous mélangeons tout et nous obtenons une solution verdâtre. De l'aluminium pré-préparé y est ajouté. Le mélange commencera à mousser - c'est de l'hydrogène. L'aluminium remplace le cuivre, et vous pouvez le voir de vos propres yeux par l'éclosion d'une teinte rougeâtre sur les matières premières d'aluminium. Une suspension blanchâtre apparaît, c'est ici que vous pouvez commencer à collecter l'hydrogène dont nous avons besoin.
Dans le processus, une chaleur supplémentaire est obtenue; en chimie, un tel processus est appelé exothermique. Il est clair que si le processus n'est pas contrôlé, il se produira quelque chose comme un geyser, qui crachera des portions d'eau bouillante, de sorte que la concentration initiale doit être contrôlée. Pour cela, un bouchon avec un tube est utilisé pour évacuer en toute sécurité l'hydrogène vers l'extérieur. Soit dit en passant, le diamètre du tube ne doit en aucun cas dépasser 8 millimètres. L'hydrogène collecté peut gonfler le ballon, qui sera beaucoup plus léger que l'air environnant, ce qui signifie qu'il lui permettra de remonter. Honnêtement, de telles expériences doivent être pratiquées avec beaucoup de soin et de prudence, sinon les blessures et les brûlures ne peuvent être évitées.
L'INVENTION A LES AVANTAGES SUIVANTS
La chaleur obtenue par l'oxydation des gaz peut être utilisée directement sur site, et l'hydrogène et l'oxygène sont obtenus à partir de l'élimination des vapeurs et des eaux de process.
Faible consommation d'eau lors de la production d'électricité et de chaleur.
La simplicité du chemin.
Économies d'énergie significatives il est consacré uniquement à réchauffer le démarreur au régime thermique établi.
Productivité élevée du processus, car la dissociation des molécules d'eau dure des dixièmes de seconde.
Explosion et sécurité incendie de la méthode, car dans sa mise en œuvre, il n'y a pas besoin de conteneurs pour recueillir l'hydrogène et l'oxygène.
Pendant le fonctionnement de l'installation, l'eau est purifiée à plusieurs reprises, transformée en eau distillée. Cela élimine les sédiments et le calcaire, ce qui augmente la durée de vie de l'installation.
L'installation est en acier ordinaire; à l'exception des chaudières en aciers résistants à la chaleur avec revêtement et blindage de leurs parois. Autrement dit, aucun matériau spécial coûteux n'est requis.
L'invention peut trouver une application dans
l'industrie en remplaçant les hydrocarbures et le combustible nucléaire dans les centrales électriques par de l'eau bon marché, largement répandue et respectueuse de l'environnement, tout en maintenant la puissance de ces centrales.
Vue alternative
Le modèle d'utilité concerne l'électrochimie et, plus spécifiquement, l'énergie hydrogène et peut être utile pour obtenir un mélange de carburant à haute teneur en hydrogène à partir de toute solution aqueuse.
Dispositifs connus pour la décomposition électrochimique directe (dissociation) de l'eau et des solutions aqueuses en hydrogène et oxygène par passage d'un courant électrique à travers l'eau. Leur principal avantage est leur facilité de mise en œuvre. Les principaux inconvénients du dispositif prototype de générateur d'hydrogène connu sont une faible productivité, une consommation d'énergie importante et un faible rendement. Le calcul théorique de l'électricité nécessaire à la production de 1 m3 d'hydrogène à partir d'eau est de 2,94 kWh, ce qui rend encore difficile l'utilisation de cette méthode de production d'hydrogène comme carburant respectueux de l'environnement dans les transports.
—
L'appareil le plus proche (prototype) de par la conception et le même objectif que le modèle d'utilité revendiqué par une combinaison de caractéristiques est un électrolyseur bien connu - le générateur d'hydrogène le plus simple contenant une chambre creuse avec une solution aqueuse (eau), des électrodes placées à l'intérieur et une source d'électricité qui leur sont connectés (livre. Encyclopédie chimique ", v. 1, m., 1988, p. 401)
L'essence du prototype - le générateur d'hydrogène connu consiste en la dissociation électrolytique de l'eau et des solutions aqueuses sous l'action d'un courant électrique sur H2 et O2.
Manque de prototype consiste en une faible productivité d'hydrogène et une consommation d'énergie importante.
Le but de la présente invention est la modernisation du dispositif pour améliorer son efficacité énergétique
Résultat technique, de ce modèle d'utilité consiste en l'amélioration technique et énergétique du dispositif connu, nécessaire pour atteindre cet objectif.
Résultat technique spécifié est obtenu par le fait que le dispositif connu contenant une chambre creuse avec une solution aqueuse, des électrodes placées dans l'eau, une source électrique qui leur est reliée, est complété par des capillaires placés verticalement dans l'eau, avec des extrémités supérieures au-dessus du niveau de l'eau, et les électrodes sont réalisés à plat, dont l'un est placé sous les capillaires, et la deuxième électrode est en treillis et est située au-dessus d'eux, et la source d'alimentation est en haute tension et réglable en amplitude et en fréquence, et l'écart entre les extrémités des capillaires et de la deuxième électrode et les paramètres de l'électricité fournie aux électrodes sont choisis en fonction de la condition d'assurer une productivité maximale de l'hydrogène, et la capacité des régulateurs est le régulateur de tension de ladite source et le régulateur de l'écart entre les capillaires et la deuxième électrode, et le dispositif est également complété par deux générateurs d'ultrasons, dont l'un est situé sous l'extrémité inférieure de ces capillaires et le second - au-dessus de leur extrémité supérieure, et le dispositif L'unité est également complétée par un dissociateur électronique de molécules de brouillard d'eau activées contenant une paire d'électrodes situées au-dessus de la surface du liquide, avec leurs plans perpendiculaires à la surface du liquide, et connectés électriquement à un générateur électronique supplémentaire d'impulsions haute fréquence à haute tension. avec une fréquence et un rapport cyclique réglables, dans la gamme de fréquences chevauchant les fréquences d'excitation résonnante des molécules évaporées d'un liquide et de ses ions.
Vidéo promotionelle:
DESCRIPTION DE L'APPAREIL DANS LE STATIQUE
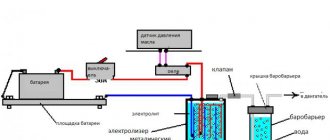
Dispositif de production d'hydrogène à partir d'eau (Fig. 1) se compose d'un récipient diélectrique 1, dans lequel est versée une solution aqueuse de liquide 2, d'un matériau capillaire finement poreux 3, partiellement immergé dans ce liquide et pré-humidifié dans celui-ci. Ce dispositif comprend également des électrodes métalliques haute tension 4, 5 , placée aux extrémités des capillaires 3, et connectée électriquement aux bornes d'une source régulée haute tension d'un champ électrique de signe constant 10, et l'une des électrodes 5 est réalisée sous la forme d'une plaque à aiguille perforée, et est positionnée de manière mobile au-dessus de l'extrémité des capillaires 3, par exemple, parallèlement à celle-ci à une distance suffisante pour éviter un claquage électrique de la mèche mouillée 3. Une autre électrode haute tension 4 est placée dans le liquide parallèlement à l'extrémité inférieure du capillaire, par exemple en matériau poreux 3 Le dispositif est complété par deux générateurs d'ultrasons 6, dont l'un est situé dans le liquide 2, presque au fond du récipient 1, et le second est situé au-dessus du niveau du liquide, par exemple en maille électrode 5.
Le dispositif contient également un dissociateur électronique de molécules de brouillard d'eau activé, constitué de deux électrodes 7,8, situées au-dessus de la surface du liquide, avec leurs plans perpendiculaires à la surface du liquide, et connectées électriquement à un générateur électronique supplémentaire 9 impulsions haute tension haute fréquence à fréquence et rapport cyclique réglables, dans la gamme de fréquences qui chevauchent les fréquences de résonance d'excitation des molécules évaporées du liquide et de ses ions.Le dispositif est également complété par une cloche 12, située au-dessus du réservoir 1 - un collecteur de gaz de collecte 12, au centre duquel se trouve un tuyau de sortie pour soutirer le gaz combustible et H2 vers les consommateurs. En substance, l'ensemble de dispositif contenant les électrodes 4,5 des unités haute tension 10 et l'ensemble capillaire 3 4, 5, 6 est un dispositif combiné d'une pompe électroosmotique et d'un évaporateur électrostatique de liquide 2 du récipient 1 ... de 0 à 30 kV / cm. L'électrode 5 est constituée d'un métal perforé ou maillé pour offrir la possibilité de passage sans entrave du brouillard d'eau et du gaz combustible formés à partir de l'extrémité des capillaires 3. Le dispositif comporte des régulateurs et des dispositifs pour changer la fréquence des impulsions et leur amplitude et cycle de service, ainsi que pour changer la distance et la position de l'électrode 5 par rapport à la surface de l'évaporateur capillaire 3 (ils ne sont pas représentés sur la figure 1).
DESCRIPTION DU DISPOSITIF DE FONCTIONNEMENT DE L'APPAREIL (FIG.1)
Tout d'abord, une solution aqueuse est versée dans le récipient 1, par exemple de l'eau activée ou un mélange eau-carburant (émulsion) 2, l'évaporateur capillaire 3-poreux en est pré-humidifié. Ensuite, une source de tension haute tension 10 est activée et une différence de potentiel haute tension est fournie à l'évaporateur capillaire 3 à travers les électrodes 4,5, et l'électrode perforée 5 est placée au-dessus de la surface de la face d'extrémité des capillaires. 3 à une distance suffisante pour éviter une panne électrique entre les électrodes 4,5. En conséquence, le long des fibres des capillaires 3 sous l'action des forces électroosmotiques et, en fait, électrostatiques d'un champ électrique longitudinal, les amas d'eau sont partiellement rompus et triés en taille, absorbés dans les capillaires 3. De plus, les molécules liquides polarisées dipolaires se déploient le long du vecteur de champ électrique et se déplacer du récipient vers les capillaires d'extrémité supérieure 3 au potentiel électrique opposé de l'électrode 5 (électroosmose). Puis ils, sous l'action de forces électrostatiques, sont arrachés par ces forces de champ électrique de la surface de la face d'extrémité du capillaire 3 - essentiellement un évaporateur électroosmotique et se transforment en un brouillard d'eau électrifié polarisé partiellement dissocié. Ce brouillard d'eau au-dessus de l'électrode 5 est ensuite également traité de manière intensive avec un champ électrique haute fréquence transversal pulsé créé entre les électrodes transversales 7,8 par un générateur électronique haute fréquence 9. En cours de collision intense de molécules dipolaires évaporées et d'eau amas au-dessus du liquide avec des molécules d'air et d'ozone, des électrons dans la zone d'ionisation entre les électrodes 7, 8, une dissociation intensive supplémentaire (radiolyse) du brouillard d'eau activé se produit avec la formation d'un gaz combustible combustible. En outre, ce gaz combustible obtenu s'écoule indépendamment vers le haut dans la cloche de collecte de gaz 12 puis à travers la sortie 13 est fourni aux consommateurs pour préparer un mélange de carburant synthétique, par exemple, dans le conduit d'admission des moteurs à combustion interne et le fournir à la combustion. chambres d'un véhicule automobile. La composition de ce gaz combustible comprend des molécules d'hydrogène (H2), d'oxygène (O2), de vapeur d'eau, de brouillard (H2O), ainsi que des molécules organiques activées évaporées dans le cadre d'autres additifs hydrocarbonés. Auparavant, l'opérabilité de ce dispositif a été montrée expérimentalement et il a été constaté que l'intensité du processus d'évaporation et de dissociation des molécules de solutions aqueuses dépend et change de manière significative en fonction des paramètres du champ électrique des sources9,10. (Intensité, puissance), sur la distance entre les électrodes 4, 5, sur la zone de l'évaporateur capillaire 3, sur le type de liquide, la taille des capillaires et la qualité du matériau capillaire 3.Les régulateurs disponibles dans l'appareil vous permettent d'optimiser les performances du gaz combustible en fonction du type et des paramètres de la solution aqueuse et de la conception spécifique de cet électrolyseur. Étant donné que dans cet appareil, une solution aqueuse d'un liquide s'évapore intensivement et se dissocie partiellement en H2 et O2, sous l'action de l'électroosmose capillaire et des ultrasons, puis se dissocie activement en raison de collisions intenses de molécules de la solution aqueuse évaporée au moyen d'un champ électrique résonnant transverse supplémentaire, un tel dispositif de production d'hydrogène et de gaz combustible consomme peu d'électricité et est donc beaucoup plus économique par dizaines de centaines de fois plus économique que les générateurs d'hydrogène à électrolyse connus.
RÉCLAMER
Dispositif à ultrasons pour produire de l'hydrogène à partir de toute solution aqueuse, contenant un récipient contenant une solution aqueuse, des électrodes métalliques placées à l'intérieur et une source d'électricité qui y est connectée, caractérisé en ce queil est complété par des capillaires placés verticalement dans cette chambre, avec leurs extrémités supérieures au-dessus du niveau de la solution aqueuse, et l'une des deux électrodes est placée dans le liquide sous les capillaires, et la deuxième électrode est rendue mobile et quadrillée et placée au-dessus eux, et la source d'alimentation est en haute tension et réglable en amplitude et en fréquence, et le dispositif est également complété par deux générateurs d'ultrasons, dont l'un est situé sous l'extrémité inférieure de ces capillaires et le second est situé au-dessus de leur extrémité, et le dispositif est également complété par un dissociateur électronique résonnant de molécules de brouillard d'eau activées contenant une paire d'électrodes situées au-dessus de la surface du liquide, avec leurs plans, perpendiculaires à la surface du liquide, et connectés électriquement à un générateur électronique supplémentaire de impulsions haute tension haute fréquence avec une fréquence et un rapport cyclique réglables, dans la gamme de fréquences contenant les fréquences d'excitation résonnante des molécules de liquide évaporées et ses ions.
RÉCLAMER
Procédé de production d'hydrogène et d'oxygène à partir de vapeur d'eau
, comprenant le passage de cette vapeur à travers un champ électrique, caractérisés en ce qu 'ils utilisent de la vapeur d'eau surchauffée avec une température
500 à 550 o C
, passé à travers un champ électrique à courant continu à haute tension pour dissocier la vapeur et la séparer en atomes d'hydrogène et d'oxygène.
J'ai longtemps voulu faire une chose similaire. Mais d'autres expériences avec une batterie et une paire d'électrodes n'ont pas eu lieu. Je voulais faire un appareil à part entière pour la production d'hydrogène, en quantité pour gonfler un ballon. Avant de fabriquer un appareil à part entière pour l'électrolyse de l'eau à la maison, j'ai décidé de tout vérifier sur le modèle.
Le schéma général de l'électrolyseur ressemble à ceci.
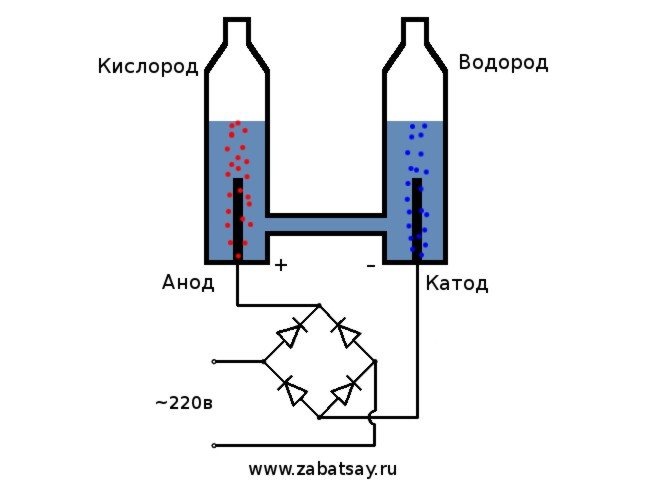

Ce modèle ne convient pas pour une utilisation quotidienne complète. Mais nous avons réussi à tester l'idée.
J'ai donc décidé d'utiliser du graphite pour les électrodes. Une excellente source de graphite pour les électrodes est le collecteur trolleybus. Il y en a beaucoup qui traînent aux fins de course. Il faut se rappeler que l'une des électrodes va s'effondrer.


Nous avons vu et finalisé avec un fichier. L'intensité de l'électrolyse dépend de la force du courant et de la surface des électrodes.


Les fils sont attachés aux électrodes. Les fils doivent être soigneusement isolés.


Pour le cas du modèle de cellule électrolytique, les bouteilles en plastique conviennent tout à fait. Des trous sont faits dans le couvercle pour les tuyaux et les fils.


Tout est soigneusement enduit de scellant.


Les goulots de bouteille coupés conviennent pour connecter deux récipients.


Ils doivent être assemblés et la couture doit être fondue.


Les écrous sont fabriqués à partir de capsules de bouteilles.


Les trous sont réalisés dans deux bouteilles au fond. Tout est connecté et soigneusement rempli de mastic.


Nous utiliserons un réseau domestique 220V comme source de tension.Je tiens à vous avertir que c'est un jouet assez dangereux. Donc, si vous n'avez pas les compétences suffisantes ou s'il y a des doutes, il vaut mieux ne pas répéter. Dans le réseau domestique, nous avons un courant alternatif, pour l'électrolyse il doit être redressé. Un pont de diodes est parfait pour cela. Celui de la photo n'était pas assez puissant et s'est rapidement éteint. La meilleure option était le pont de diodes chinois MB156 dans un boîtier en aluminium.


Le pont de diodes devient très chaud. Un refroidissement actif sera nécessaire. Un refroidisseur pour un processeur d'ordinateur est parfait. Une boîte de jonction de taille appropriée peut être utilisée pour le boîtier. Vendu en électroménager.


Plusieurs couches de carton doivent être placées sous le pont de diodes.


Les trous nécessaires sont faits dans le couvercle de la boîte de jonction.


Voici à quoi ressemble l'unité assemblée. L'électrolyseur est alimenté par le secteur, le ventilateur est alimenté par une source d'alimentation universelle. Une solution de bicarbonate de soude est utilisée comme électrolyte. Ici, il faut se rappeler que plus la concentration de la solution est élevée, plus la vitesse de réaction est élevée. Mais en même temps, le chauffage est également plus élevé. De plus, la réaction de décomposition du sodium à la cathode contribuera au chauffage. Cette réaction est exothermique. En conséquence, de l'hydrogène et de l'hydroxyde de sodium se formeront.


L'appareil sur la photo ci-dessus était très chaud. Il fallait l'éteindre périodiquement et attendre qu'il refroidisse. Le problème de chauffage a été partiellement résolu en refroidissant l'électrolyte. Pour cela, j'ai utilisé une pompe de fontaine de table. Un long tube passe d'une bouteille à l'autre à travers une pompe et un seau d'eau froide.


La pertinence de cette question aujourd'hui est assez élevée en raison du fait que le domaine de l'utilisation de l'hydrogène est extrêmement vaste et que sous sa forme pure, il ne se trouve pratiquement nulle part dans la nature. C'est pourquoi plusieurs techniques ont été développées qui permettent l'extraction de ce gaz à partir d'autres composés par des réactions chimiques et physiques. Ceci est discuté dans l'article ci-dessus.
Le gars a fait une installation pour produire de l'hydrogène
Roman Ursu. Dans cette vidéo, je voulais montrer comment vous pouvez fabriquer un petit générateur à partir de 10 lames de rasage qui extrait l'hydrogène de l'eau. Pour commencer, vous avez besoin d'un bloc d'alimentation de 5 à 12 volts, intensité de courant de 0,5 à 2 ampères. Fils de cuivre, bocal en verre avec bouchon à vis scellé. Une bouteille en plastique, un morceau de règle en plastique. Deux compte-gouttes. 10 lames. Sel comestible. Outils: fer à souder, pistolet à colle, couteau à papeterie.


Produits pour les inventeurs